
|
|
|||||
|
||||||
6企業9批次藥品不符合規定將遭立案調查!摘要:
醫藥網5月25日訊 5月24日,國家藥品監督管理局官網發布通告稱,經山西省食品藥品檢驗所等2家藥品檢驗機構檢驗,標示為北京同仁堂(亳州)飲片有限責任公司等6家企業生產的9批次藥品不符合規定。具體情況如下:
經山西省食品藥品檢驗所檢驗,標示為北京同仁堂(亳州)飲片有限責任公司、亳州市佰世信中藥飲片有限公司、亳州市永剛飲片廠有限公司等5家企業生產的7批次薄荷不符合規定,不符合規定項目包括性狀、顯微特征、薄層色譜。
經吉林省藥品檢驗所檢驗,標示為藥都制藥集團股份有限公司生產的1批次木香順氣丸不符合規定,不符合規定項目為性狀。
經山西省食品藥品檢驗所檢驗,標示為亳州市佰世信中藥飲片有限公司生產的1批次羌活不符合規定,不符合規定項目為特征圖譜。
9批次不符合規定藥品名單
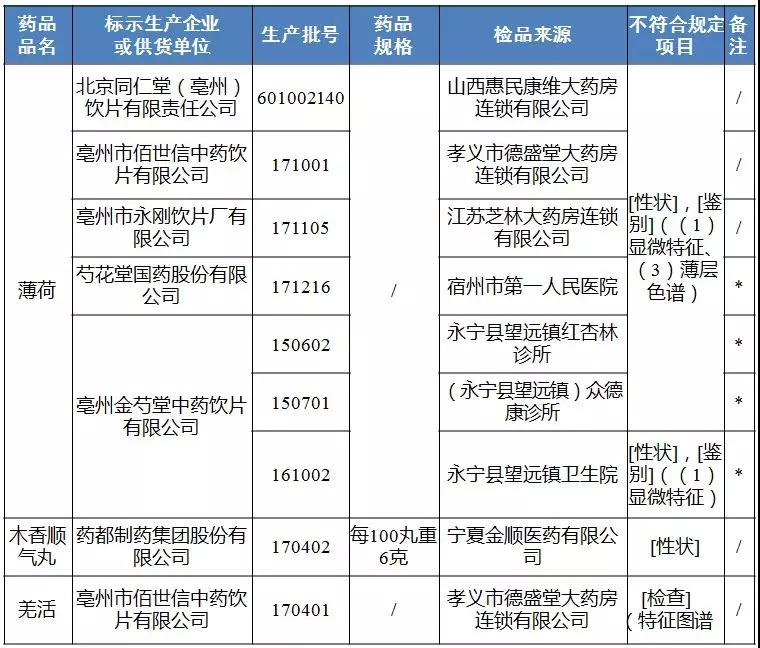 備注:標“*”的藥品為標示生產企業否認為該企業生產
國家藥品監督管理局要求相關省級藥品監督管理部門對上述企業和單位依據《中華人民共和國藥品管理法》第七十三、七十四、七十五條等規定對生產銷售假劣藥品的違法行為進行立案調查,自收到檢驗報告書之日起3個月內完成對相關企業或單位的調查處理并公開處理結果。
在立案調查工作中,企業對產品真實性有異議的,可以向所在地省級藥品監督管理部門提出。標示生產企業所在地省級藥品監督管理部門應對該企業的生產銷售情況進行調查核實,被抽樣單位所在地省級藥品監督管理部門應追溯問題產品來源;兩地藥品監督管理部門要相互配合、及時通報、一查到底,并將相關工作情況按要求及時上報。
|
|
Copyright ?2015 廣東穗康醫藥有限公司
粵ICP備15022662號(粵)
-技術支持:信息管理部|聯系我們
|